¿Qué dice la ley de Richter
Las masas de dos elementos diferentes que se combinan con una misma cantidad de un tercer elemento, guardan la misma relación que las masas de aquellos elementos cuando se combinan entre sí.
¿Que enuncia la ley de Richter?
La ley de las proporciones recíprocas de la siguiente manera: las masas de los elementos que se combinan con una masa de un tercero, guardan la misma proporción que las masas de los dos cuando se combinan entre sí.
¿Que enuncia la ley de la conservación de la masa?
La Ley de la conservación de la ma- teria: “En toda reacción química la masa se conserva, es decir, la masa total de los reactivos es igual a la masa total de los productos”.
¿Que explica la ley de las proporciones reciprocas de Richter?
Ley de las proporciones recíprocas. Concepto: Los pesos de diferentes elementos que se combinan con un mismo peso de un elemento dado, dan la relación de pesos de estos Elementos cuando se combinan entre sí o bien múltiplos o submúltiplos de estos pesos.¿Cuál es la ley de las proporciones multiples?
Esta ley afirma que cuando dos elementos se combinan para originar distintos compuestos, dada una cantidad fija de uno de ellos, las diferentes cantidades del otro que se combinan con dicha cantidad fija para dar como producto los compuestos, están en relación de números enteros sencillos.
¿Cuál es la ley de la combinacion de volúmenes?
En 1808 Louis Joseph Gay-Lussac formuló la Ley de los volúmenes de combinación, la cual reza lo siguiente: en cualquier reacción química los volúmenes de todas las sustancias gaseosas que intervienen en la misma están en una relación de números enteros sencillos.
¿Qué dice la ley de las proporciones reciprocas o de Richter Wenzel?
El enunciado de la ley es el siguiente: Las masas de dos elementos diferentes que se combinan con una misma cantidad de un tercer elemento, guardan la misma relación que las masas de aquellos elementos cuando se combinan entre sí.
¿Cómo se aplica la ley dela conservacion dela materia en la vida diaria?
- La descomposición de la fruta. Es notable la reducción del tamaño del alimento a medida que se degrada. …
- Fundir hielo. Al dejar un vaso con hielo a temperatura ambiente el hielo se derrite. …
- Hervir agua. …
- Objetos oxidados. …
- Formación de compuestos.
¿Cuál es la ley de los volúmenes de combinacion?
La ley de los volúmenes de combinación establece que, en una reacción en la que la temperatura y la presión son constantes, los volúmenes de todos los gases que participan en ella guardan entre sí una relación sencilla.
¿Quién creó la ley de las proporciones definidas?El químico francés Joseph Louis Proust permaneció 13 años como profesor de química y metalurgia en el Real Colegio de Artillería de Segovia.
Article first time published on¿Qué dice la ley de las proporciones definidas ejemplos?
Cuando los elementos se combinan para formar compuestos siempre es necesaria la misma proporción de masas de los constituyentes para hacer un compuesto en concreto. Por ejemplo, 23,0 g de sodio siempre se combinan con 35,5 g de cloro para producir 58,5 g de cloruro sódico (NaCl, sal común).
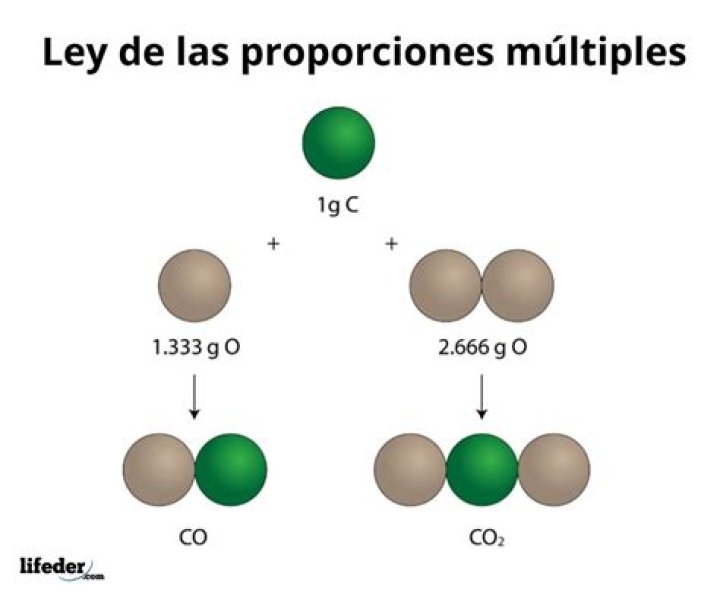
¿CómO se aplica la ley de las proporciones múltiples para la formación de los compuestos monóxido de carbono y dióxido de carbono?
“Cuando dos o más elementos se combinan para formar más de un compuesto, la masa de uno de ellos, que se une a la masa fija del otro, está en relación de números enteros y sencillos” Ejemplo: El carbono y el oxígeno forman dos compuestos diferentes CO2 Dióxido de carbono. CO Monóxido de carbono.
¿Quién es Jeremias Benjamín Richter?
Jeremias Benjamin Richter (1762-1807) fue un químico alemán. A él se le debe la noción de peso equivalente y la ley que lleva su nombre: Los elementos se combinan en proporción a sus pesos equivalentes, multiplicados por números enteros y pequeños.
¿Cuando los gases reaccionan entre sí para formar otros gases y todos los volúmenes se miden a la misma temperatura y presión?
En 1808, Gay-Lussac publicó que los gases reaccionan entre sí combinándose y obteniéndose volúmenes en proporción a números enteros pequeños. La explicación que se propuso era que volúmenes iguales de gases a la misma temperatura y presión contienen números iguales de átomos.
¿Cómo se clasifican las reacciones químicas?
Las reacciones químicas se clasifican por la energía que requieren o liberan, o bien por el proceso a que se someten los reactivos. Se presenta una síntesis de la reacción química exotérmica y endotérmica, síntesis y descomposición.
¿Quién enunció lo siguiente el volumen de la combinación de los gases debe ser inferior o igual a la suma de los volúmenes de las sustancias gaseosas que se combinan?
GAY-LUSSAC observó que el volumen de la combinación gaseosa resultante era inferior o a lo más igual a la suma de los volúmenes de las substancias gaseosas que se combinan.
¿Qué relación hay entre los coeficientes estequiométricos y los volúmenes de combinación?
Cuando todos los reactivos y productos sean gases en las mismas condiciones de presión y temperatura, se cumple que la relación entre los volúmenes de las sustancias que intervienen es la expresada por los coeficientes estequiométricos. Ley de los volúmenes de combinación de Gay-Lussac.
¿Qué representa el coeficiente estequiométrico en una ecuación química?
Son los números que aparecen delante de las fórmulas de los reactivos y productos después de igualar la ecuación química. … Los coeficientes estequiométricos indican en qué proporción intervienen en la reacción las cantidades (número de moles) de reactivos y de productos de la reacción.
¿Cómo demostrar la ley dela conservacion dela materia?
El Peso Molecular permite comprobar si se cumple la Ley de Conservación de la Materia, o Ley de Lavoisier, ya que en una reacción química la suma de la masa de los reactantes debe ser igual a la suma de la masa de los productos. Masa Atómica: H= 1u, O= 16u.
¿Qué dice la segunda ley de las proporciones fijas y quién lo planteó?
La ley de Proust, una de las leyes fundamentales de la química, fue enunciada en 1801 para dar respuesta a la forma en la que se combinan dos o más elementos. … Es decir, los elementos que lo conforman mantienen una proporción fija en peso para cualquier muestra pura de un compuesto.
¿Cuál es la importancia de la ley de las proporciones definidas?
Enunciada por el científico Proust, esta ley mantiene que al combinarse dos o mas elementos para hacer un compuesto determinado, las masas de las sustancias que intervienen son fijas.
¿Qué crees que se forma cuando dos o más elementos se combinan?
Cuando dos o mas elementos se combinan en proporciones de masa definidas forman un compuesto químico. A esta representación se le conoce como formula química.
¿Cuánto cuesta el dióxido de carbono?
Precios CO2EUACEREnero33,43 €0,37 €Febrero37,89 €0,39 €Marzo40,87 €0,42 €Abril45,22 €0,60 €
¿Qué hizo Lavoisier en la tabla periodica?
Antoine Lavoisier identificó más de 20 elementos químicos y clasificó en metales, no metales, metales de transición y metaloides, en 1789 publicó una lista de 33 elementos químicos. … En esta tabla los elementos se ordenaron de izquierda a derecha de forma horizontal y en siete columnas.
¿Qué hizo Meyer en la tabla periodica?
Maiella Ramos Meyer es mejor conocido por su participación en la clasificación periódica de los elementos. Observó que si los elementos están dispuestos en el orden de sus pesos atómicos se clasifican en grupos que repiten propiedades químicas y físicas similares , a intérvalos periódicos.
¿Qué es el volumen cómo se mide y cuál es su relación con la ley de volúmenes de combinación?
Lussac formuló en 1808 la Ley de los volúmenes de combinación que lleva su nombre, la cual puede enunciarse como sigue: en cualquier reacción química los volúmenes de todas las sustancias gaseosas que intervienen en la misma están en una relación de números enteros sencillos. …
¿Cómo está relacionada el número de Avogadro con el volumen molar?
Por número de Avogadro se entiende al número de entidades elementales (es decir, de átomos, electrones, iones, moléculas) que existen en un mol de cualquier sustancia. … La ecuación sería la siguiente: 1 mol = 6,022045 x 10 elevado a 23 partículas.
¿Cuándo reaccionan gases bajo condiciones de temperatura y presión equivalentes lo hacen en relaciones de volúmenes de números enteros y sencillos?
En 1809, Gay-Lussac estableció esta ley y planteó que «cuando reaccionan gases bajo condiciones de temperatura y presión equivalentes, lo hacen en relaciones de volúmenes de números enteros y sencillos».



